|
关于r/r B-ALL
“明明 CD19 CAR-T 能让 60%-80% 的复发难治 B 细胞急性淋巴细胞白血病(r/r B-ALL)患者有应答,可细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)这两大毒性,却像两座大山,把很多患者拦在治疗门外。”
在临床中,我们见过太多这样的遗憾 —— 就像 ZUMA-3 研究里,93% 的患者用 KTE-X19 治疗后出现 CRS,31% 是≥3 级的严重反应,78% 出现 ICANS,38% 达到 3 级及以上,这些数字背后,是患者和家属的煎熬。
而这一切的关键,绕不开白细胞介素 - 6(IL-6)。它不仅是 CRS 的核心细胞因子,还会通过影响血脑屏障、协同 IL-1、粒细胞 - 巨噬细胞集落刺激因子(GM-CSF)等,间接加重 ICANS。更麻烦的是,CAR-T 细胞自身分泌的 IL-6,还会触发单核细胞释放更多 IL-6,形成 “毒性循环”。虽然托珠单抗能治 CRS,但它难穿透血脑屏障,对 ICANS 几乎没用。
难道就没有办法平衡疗效和毒性吗?
在不断的探索和研发下,优卡迪生物开发了新型ssCART-19细胞,通过shRNA技术沉默IL-6表达,既能大幅减少单核细胞释放 IL-6,又不影响 CAR-T 的抗肿瘤能力,并在苏州大学附属第一医院开展了一项 I 期研究,近日发表于《Blood Cancer Journal》。

研究中患者入组流程图
1 一场针对 “毒性” 的 Phase 1 试验从设计到入组
为明确 ssCART-19 的安全性和有效性,单中心、单臂的 1 期临床试验启动,研究对象为 18-65 岁的 r/r B-ALL 患者。这些患者需满足关键条件:骨髓原始细胞比例≥5%、流式检测到 CD19 表达、体力状态(ECOG)0-1 级、器官功能良好,毕竟经过前期治疗,患者身体本就脆弱,安全必须放在首位。
治疗前的准备至关重要:患者会在 CAR-T 回输前 5-3 天,接受氟达拉滨(30mg/m²/ 天)联合环磷酰胺(300mg/m²/ 天)的清淋治疗,为 CAR-T 细胞 “铺路”;回输时也特意分次进行,将总剂量分成 10%、30%、60% 逐步输注,以降低急性反应风险。
试验分为两阶段:先进行剂量爬坡,设置低(1×10⁶细胞 /kg)、中(5×10⁶细胞 /kg)、高(1×10⁷细胞 /kg)三个剂量组,纳入 6 例患者;再根据爬坡阶段的安全和疗效数据,确定 2 期推荐剂量后进入扩展阶段。
2021 年 4 月至 2023 年 10 月期间,共筛查 31 例患者,10 例因不符合条件被排除,21 例成功入组并完成细胞采集 —— 幸运的是,所有患者的 ssCART-19 均制备成功。不过,有 4 例患者未能接受回输:2 例因肺部感染无法控制,1 例因脑出血,1 例因疾病快速进展,最终 17 例患者顺利接受治疗。
研究中患者入组流程图
2 试验结果超预期毒性大降且疗效稳固
试验结果令人惊喜 ——ssCART-19 真的打破了 “高效必高毒” 的困局。
先看安全性:17 例患者里,没有出现任何剂量限制性毒性(DLT) 。虽然所有人都有至少 1 种治疗相关不良反应,但严重反应主要在血液系统:94.1% 的患者有 3 级及以上淋巴细胞减少,88.2% 有中性粒细胞减少和白细胞减少,70.6% 有贫血,58.8% 有血小板减少。有 2 例患者因回输后持续中性粒细胞减少引发感染性休克去世,这也提醒我们,后续要加强粒细胞缺乏期的感染防控。
最让人惊喜的是 CRS 和 ICANS 的控制——
CRS 发生率 76.5% ,但仅 17.6%(3 例)是 3 级,没有 4 级 CRS。低剂量组(不管是爬坡还是扩展阶段)3 级 CRS 发生率才 10%,远低于常规 CD19 CAR-T(比如 ZUMA-3 里 31% 的≥3 级 CRS)。而且所有 CRS 患者,用托珠单抗、糖皮质激素或两者联用后都快速缓解,哪怕是骨髓原始细胞比例达 49% 的高肿瘤负荷患者,也没出现更重的 CRS。
没有任何患者出现 ICANS ,包括那例有 CNSL 的患者!要知道常规 CAR-T 治疗中 ICANS 发生率常超 50%,这一点突破对中枢受侵犯的患者来说太重要了。 更意外的是,我们没发现 ssCART-19 剂量和 CRS 严重程度、细胞因子峰值有关联 —— 这意味着低剂量下,它也能在控毒的同时发挥作用。
再看疗效:3 个月时,17 例患者里 11 例(64.7%)达到客观缓解(ORR) ,其中 8 例(47.1%)是完全缓解(CR),3 例(17.6%)是不完全血液学恢复的完全缓解(CRi),而且所有缓解患者的微小残留病(MRD)都是阴性 —— 这可是长期生存的关键指标。
不同剂量组表现有差异:低剂量组最亮眼,爬坡阶段 3 例全缓解(100%),扩展阶段 7 例里 4 例缓解,整体 ORR 达 80%;中剂量组 6 例里 4 例缓解(66.7%);高剂量组仅 1 例,没缓解。这也让我们确定,低剂量(1×10⁶细胞 /kg)就是后续 2 期试验的推荐剂量。
随着随访延长(中位随访 20.1 个月),疗效数据更让人振奋:达到 CR/CRi 的 14 例患者,中位缓解持续时间(DOR)25.8 个月;低剂量组里达 CR/CRi 的患者,中位 DOR 21.3 个月;所有患者中位无进展生存期(PFS)22.2 个月,总生存期(OS)还没达到;中剂量组有 4 例患者在回输后中位 5 个月接受了异基因造血干细胞移植(allo-HSCT),为长期生存再加了层保障。
其中有一个关键性发现:达 CR/CRi 的患者,ssCART-19 细胞扩增水平更高,回输后 28 天内的细胞浓度曲线下面积(AUC₀₋₂₈d)也更大;而复发的患者,疾病进展时已经测不到 CAR-T 细胞了 —— 这说明 CAR-T 细胞持续存在,是维持缓解的关键。
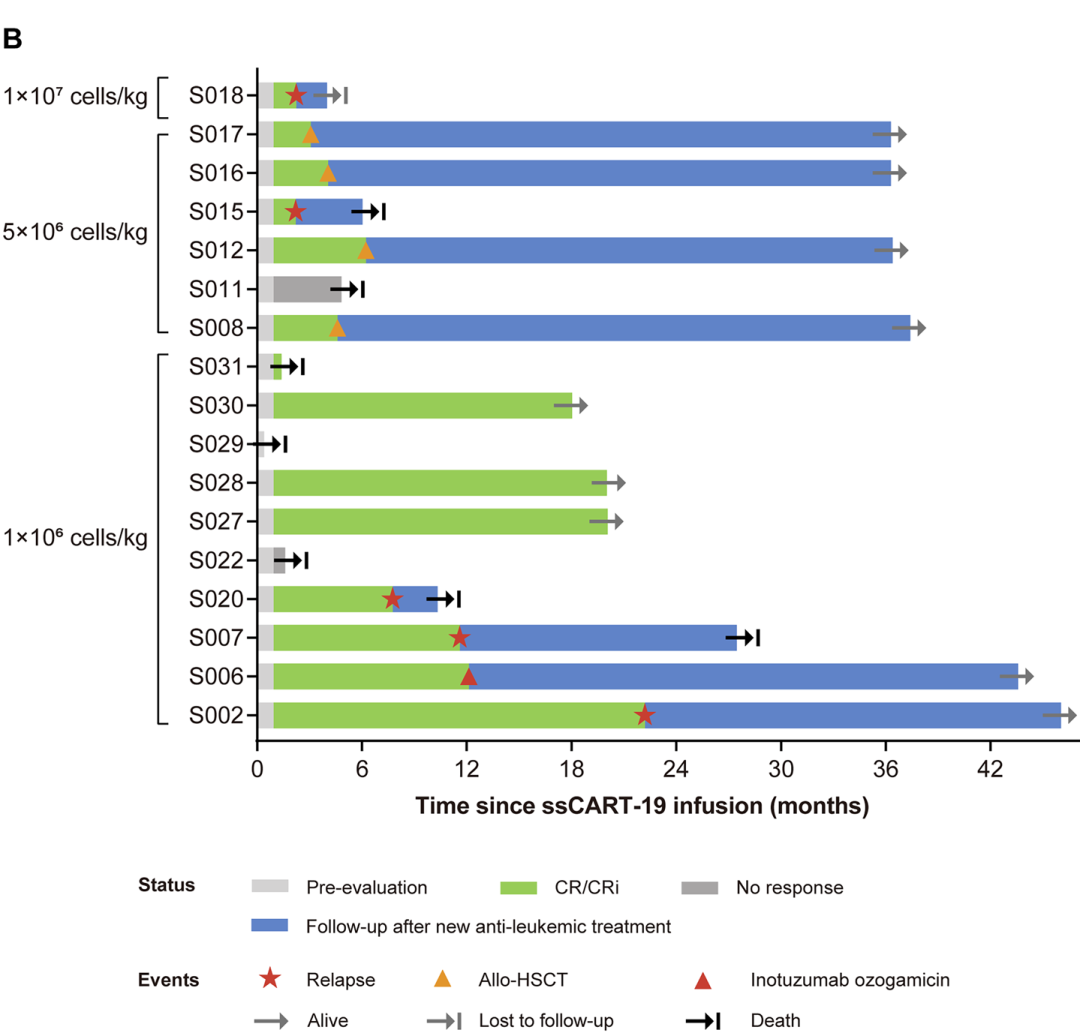
个体患者临床反应与随访的泳道图
总结
未来值得期待 ,为更多高危患者打开生存通道! 回头看整个试验,ssCART-19 的价值不只是 “降毒性”,更在于它给 “高危患者” 带来了希望 —— 比如高肿瘤负荷、中枢侵犯、有高危基因、不能耐受高剂量CAR-T者,过去他们可能因怕毒性不敢试 CAR-T,现在有了新选择。
当然试验有局限:单中心、样本量小,未来需要多中心、更大规模的 2 期试验验证;随访时间还不够长,得更久的数据确认持久获益;而且血液学毒性和感染风险仍需重视,后续要优化支持治疗。
但从 1 期结果来看,ssCART-19 已经展现出 “低毒高效” 的潜力,它通过敲低 IL-6 调控毒性的思路,也为其他 CAR-T 疗法优化提供了参考。我们相信,随着研究深入,会有更多像 ssCART-19 这样的疗法出现,让 r/r B-ALL 患者不仅能 “活下去”,还能 “活得好”。
一项多中心2期临床试验正在进行中,以在更大队列中进一步验证低剂量ssCART-19的疗效和安全性(剂量为1×10⁶ CAR-T cells/kg)。
参考文献: Xue, SL., Liu, MJ., Qian, CS. et al. Blood Cancer J. 15, 182 (2025). 扫码可之家下载文献原文
|